-
1
填写账户信息
-
2
填写基本信息
-
3
注册成功
-
网站首页
-
产品中心
- 小分子分离色谱柱
-
反相色谱柱
ChromCore 120 C18色谱柱 ChromCore AQ C18色谱柱 ChromCore C18色谱柱 ChromCore AR C18色谱柱 ChromCore BR C18色谱柱 ChromCore Polar C18色谱柱 ChromCore C8色谱柱 ChromCore C30色谱柱 ChromCore Phenyl色谱柱 ChromCore Phenyl-Hexyl色谱柱 ChromCore Phenyl-Ether色谱柱 ChromCore PFP色谱柱 ChromCore Biphenyl色谱柱 ChromCore 300 C4-T色谱柱 ChromCore 300 C4色谱柱
- 正相/亲水作用色谱柱
- 离子交换色谱柱
- 糖分析柱
- 专用色谱柱
- UHPLC色谱柱
- 保护柱与柱芯
-
应用中心
-
资料下载
-
服务与支持
- 知识共享
-
色谱知识
【知识分享】液相色谱如何做保养?快转发给实验室的小伙伴们 【知识分享】气相色谱实用热点问题,答案在这里! 【知识分享】少走弯路-色谱柱过载知多少? 知识分享 | 干货!液相色谱柱活化方法、维护与注意事项(下) 【知识分享】干货!液相色谱柱活化方法、维护与注意事项(上) 【知识分享】实验室常用单位换算公式大全,果断收藏! 【实例解析】新色谱柱出现异常峰?鬼峰小柱来破案! 【知识分享】液相色谱故障排除(一)压力问题 【知识分享】液相色谱的错误操作,快来避坑! 【知识分享】高效液相色谱(HPLC)方法的开发思路经验小结 【知识分享】是时候搞清楚了!液相色谱基线不稳定、噪声升高原因排查! 【知识分享】色谱峰劈个“叉”,这些原因需知道! 【知识分享】液相色谱要么堵要么漏?原因是这个! 【知识分享】气相色谱“闹脾气”,这些方法能急救! 气相色谱的各种知识,你get到了吗?
-
仪器操作维护
【知识分享】春节假期来临,仪器节前关机&节后开机实用攻略 【知识分享】色谱达人必备-药物研究中HPLC方法开发思路及关键点 【知识分享】液相色谱的错误操作,快来避坑! 【知识分享】色谱分析中的“调节剂”缓冲盐何其重要! 【色谱知识】警惕不良习惯,排查关键问题,轻松应对液相色谱的小情绪! 【色谱知识】色谱柱柱压异常的原因及解决办法 【色谱知识】液相色谱柱安装、启用和维护中的重点注意事项 我的色谱柱怎么了?实例分析二:色谱柱寿命奇短的原因和解决办法 【应用分享】UPLC和HPLC有什么区别?选择UPLC 还是HPLC? 【色谱知识】气相色谱使用的常见问题及解决方案 【知识分享】液相色谱故障排除(一)压力问题 【知识分享】是时候搞清楚了!液相色谱基线不稳定、噪声升高原因排查! 【知识分享】高压来袭,你准备好了吗?液相色谱系统压力升高和压力不稳的原因及排除 【知识分享】体积残留、吸附残留和不完全洗脱3大残留问题探讨! 【知识分享】和载气问题说NO!气相色谱载气系统问题及解决方案!
- 样品前处理
- 案例分享
-
典型案例
【应用分享】饲料中维生素ADE的测定(在线固相萃取—二维液相色谱法) 【应用分享】食品中低聚半乳糖的测定(GB 5009.289-2023) 【应用分享】特殊医学用途配方食品中维生素ADE的含量测定 【应用分享】发酵液中2'-岩藻糖基乳糖的液相分析 【应用分享】鱼油中脂肪酸的快速气相分析 【应用分享】生活饮用水中环氧氯丙烷的提取与检测(GB/T 5750.8-2023) 【应用分享】止吐药-盐酸帕洛诺司琼的分离与检测 【应用分享】婴幼儿配方奶粉中维生素A、D和5种维生素E的含量测定 【应用分享】婴幼儿配方奶粉中维生素ADE的含量测定(GB5009.296-2023) 【应用分享】采用自动在线衍生方法分析人参和红参中游离的氨基酸 【应用分享】对此欢终宴,倾壶待曙光-三大名酒的检测 【应用分享】保健食品中免疫球蛋白IgG的提取与检测 【应用分享】新型降糖药物—达格列净中间体的检测 【应用分享】ChromCore AQ C18色谱柱助力中药配方颗粒浙江省标准方法 【应用分享】火麻仁配方颗粒中胡芦巴碱的含量测定
-
中国药典项目
【应用分享】抗癫痫药——苯妥英钠的含量测定(中国药典) 【应用分享】皮肤科用药——醋酸泼尼松龙的含量测定(中国药典) 【应用分享】麻醉药——依托咪酯的分离(中国药典) 【应用分享】中药满山红的含量测定(中国药典) 【应用分享】支气管扩张剂——多索茶碱注射液的分离(中国药典) 【应用分享】利胆药——羟甲香豆素的分离(中国药典) 【应用分享】雌激素药物雌二醇的分离(中国药典) 【应用分享】西洛他唑片中有关物质的含量测定(中国药典) 【应用分享】醋酸泼尼松的含量测定(中国药典) 【应用分享】中药西红花的含量测定(中国药典) 【应用分享】原发性高血压降压药-厄贝沙坦的检测(中国药典) 【应用分享】倍他环糊精的含量测定(中国药典) 【应用分享】中药三七的含量测定(中国药典) 【应用分享】感冒清热颗粒中葛根素的含量测定(中国药典) 【应用分享】丝裂霉素的分析和测定(中国药典)
-
中药33种农残
【应用分享】中药青蒿的33种农残测定分析 【应用分享】中药连翘的33种农残测定分析 【应用分享】中药太子参的33种农残测定分析 【应用分享】中药益母草的33种农残测定分析 【应用分享】中药石斛的33种农残测定分析 【应用分享】中药桔梗的33种农残测定分析 【应用分享】中药薄荷的33种农残测定分析 【应用分享】中药红花的33种农残测定分析 【应用分享】中药广藿香的33种农残测定分析 【应用分享】中药当归的33种农残测定分析 【应用分享】中药辛夷的33种农残测定分析 【应用分享】中药枳实的33种农残测定分析 【应用分享】中药红景天的33种农残测定分析 【应用分享】中药款冬花的33种农残测定分析 【应用分享】中药莪术的33种农残测定分析
-
样品前处理案例
【应用分享】水中17种全氟化合物的提取与检测(HJ 1333-2023) 【应用分享】食品中低聚半乳糖的测定(GB 5009.289-2023) 【应用分享】纳谱分析助力食品中乳铁蛋白测定新国标 【应用分享】食品中N-二甲基亚硝胺的提取与检测(GB 5009.26-2023) 【应用分享】食品中合成着色剂的提取与检测(GB 5009.35-2023) 【应用分享】食品中乙二胺四乙酸二钠的提取与检测 【应用分享】一柱两用——蔬菜及动物性食品中环丙氨嗪的提取与检测 【应用分享】自来水中的5种卤代乙酸的提取与检测(GB/T 5750-2023) 【应用分享】玉米面粉中赭曲霉毒素A的提取与检测 【应用分享】植物源性食品中331种农药及其代谢物残留量的测定 【应用分享】动物源性食品中利巴韦林的提取与检测 【应用分享】水果罐头中合成着色剂的提取与检测(SelectCore QMA固相萃取柱) 【应用分享】酱鸭和蜜饯中合成着色剂的检测(国标征求意见稿) 【应用分享】温中止痛中药——花椒的33种农残测定分析(固相萃取法) 巴氏杀菌乳中乳铁蛋白的提取与检测—食品中乳铁蛋白的测定(2021征求意见稿)
- 用户文献
-
色谱柱文献
Industrializable approach for preparing hydrogel microneedles and their application in melanoma treatment Determination of Aflatoxins in Peanut Oil by One-Step Solid-Phase Extraction with Metal-Organic Framework MIL-101 (Cr) Filled Syringe Filter and HPLC-MS/MS One-step purification of solid phase micro-extraction based on MIL-101(Cr) for the determination of vanillin, methyl vanillin and ethyl vanillin in edible vegetable oil samples Discovery of neo-Clerodane Diterpenoids from Ajuga campylantha as Neuroprotective Agents against Ferroptosis and Neuroinflammation_ChromeCore NH2/UniChrial CMZ 高效液相色谱-串联质谱法测定食用动物组织中那西肽残留_ChromCore C18 Dissolving microneedle loaded with azelaic acid for acne vulgaris therapy_ChromCore C18 Ferroptosis inhibitory aromatic abietane diterpenoids structural revision_ChromCore NH2 Combined effects of tranexamic acid and licorice extract_ChromCore HILIC-Amide HPLC法测定注射用盐酸头孢替安的有关物质_ChromCore AQ C18 液相色谱法测定笋制品中阿斯巴甜的含量_ChromCore C18-P 液相色谱串联质谱法测定鸡蛋...羊奶中泰乐菌素A残留的研究_ChromCore C18 体外消化对油茶蒲提取物抑制α-葡萄糖苷酶活性的影响_ChromCore AQ C18 液相色谱-质谱质谱串联法测定番茄酱中六种红曲色素_ChromCore C18 清远与肇庆巴戟天的质量比较_ChromCore 120 C18 清远市售盐制巴戟天的质量评价_ChromCore 120 C18
- 前处理产品文献
-
关于纳谱
- 新闻动态
-
公司新闻
【纳谱招聘】加入我们,一起热辣滚烫! 【纳谱资讯】3.8女神节·致敬发光的她 【网络研讨会】CACA特邀-抗体/蛋白类生物药物的色谱分离技术 恭贺新春·纳谱分析给您拜年了! 【年会回顾】纳谱分析2024年迎新会暨成立五周年年会圆满举行! @所有人 春节将至,纳谱分析提醒您年终备货,有备无患! 【年度盘点】2023热门文章排行榜!快来看看有没有你的菜 【放假通知】新年新征程,启航2024! 【纳谱资讯】治疗性蛋白药物液相色谱表征与分析研讨会成功举办! 【喜讯】纳谱分析应邀到访西交利物浦大学并签署合作备忘录 【纳谱资讯】热烈欢迎南京海关动植食中心考察团莅临纳谱分析参观交流 【喜讯】ChromCore AQ C18色谱柱助力中药配方颗粒山东省标准方法 团建之旅 | 不一样的520,和纳谱一起“趣”安吉! 纳谱分析五周年庆 | 相伴五载,感恩同行 喜讯 | 苏州纳米城启用十周年 纳谱分析荣获“闪亮新秀企业”奖项
-
展会通知
【展会通知】第二届金陵国际生物化学分析会议暨展览会 【展会通知】DIQC 2024药品质量控制与检验技术大会-石家庄站 【展会通知】IBQC 2024第三届国际生物药质量大会-苏州 【国际展会】Analytica 2024德国慕尼黑分析生化及实验室展览会 【会议通知】邀您参加中国生物药分析与质量峰会BioAQ 2024 【展会通知】BIOCHINA 2024(EBC)第九届易贸生物产业大会 【展会通知】广州站-DIQC 2024药品质量控制与检验技术大会 【国际展会】与您相约美国Pittcon 2024实验室及分析仪器展 【国际展会】俄罗斯制药设备、原料及技术展Pharmtech & Ingredients 2023 【展会通知】CPQC 2023-苏州站 2023制药行业质量管理与控制技术研讨会 【国际展会】BIOEXPO 2023土耳其生物技术及实验室设备展 【展会通知】长沙站-SPC 2023 湖南省样品前处理技术创新大会 【展会预告】DIQC 2023药品质量控制与检验技术大会-北京站 【展会通知】广州站-第14届药品质量安全大会 【国际展会】ARABLAB LIVE 2023第41届迪拜实验室展
-
新品发布
【新品来袭】3μm BioCore Glycan糖型分析色谱柱 【新品上市】1.8μm BioCore Glycan糖型分析色谱柱 【新品推介】食品中N-二甲基亚硝胺的提取与检测(GB 5009.26-2023) 【新品上市】食用盐中铅的提取与检测(GB 5009.12-2023) 【新品首发】ChromCore HILIC-ZW两性离子亲水色谱柱上市! 【重磅新品】1.8μm BioCore SEC-300色谱柱上市啦! 【新品速递】ChromCore HP C18制备柱,“柱”力小分子化合物高效分离纯化 【重磅新品】抗体片段分离利器—BioCore RP-1000色谱柱高调登场 【产品推介】ChromCore UHPLC超高效反相色谱柱火热上线! 【重磅产品】纳谱分析ChromCore SAA表面活性剂分析专用柱 【明星产品】高效体积排阻色谱柱—BioCore SEC色谱柱 【新品来袭】“手性芯”-ChiralCore手性液相色谱柱 【重磅产品】BioCore系列色谱柱-生物大分子色谱表征分析的利器 【产品推荐】这是一篇“不正经”的“正经”推文-ChromCore C30产品微信推送 【产品推荐】ChromCore PAH多环芳烃专用柱的妙用!
-
活动通知
【谱图征集】纳谱分析谱图征集活动,好礼等你拿! 【论文征集】叮,您有一份奖励请注意查收,最高1000元! 年末大促开始啦!千万别错过!!! 前处理宝典 |《植物类中药33种农残应用文集》第二版来袭!速领! 纳谱五周年 | 色谱耗材冰点价!更有精美纪念品相送! 瓜分现金红包 | 纳谱分析五周年「照片征集」活动火热开展中 庆液相色谱柱年销售破万支·集赞领好礼活动圆满结束 纳谱分析色谱柱年销售破10000支!集赞领好礼,最高赢色谱柱 温暖秋冬·倾情回馈,纳谱分析手性柱送福利啦! 纳谱分析年终钜惠大放送,Let's go,一起购! 【有奖征文】纳谱分析第三届有奖征文活动开始啦!参与即有奖,速来参与! 【金秋促销】开学钜惠!福利大放送!买就送!更多好礼等你来! 【直播预告】7月25日聚焦抗体药物下游工艺——生物大分子表征分析专场 纳谱分析助力色谱学堂《分不开怎么办》在线答疑栏目 限时申领 |《植物类中药33种农残应用文集》前处理保姆级教程
-
联系我们
-
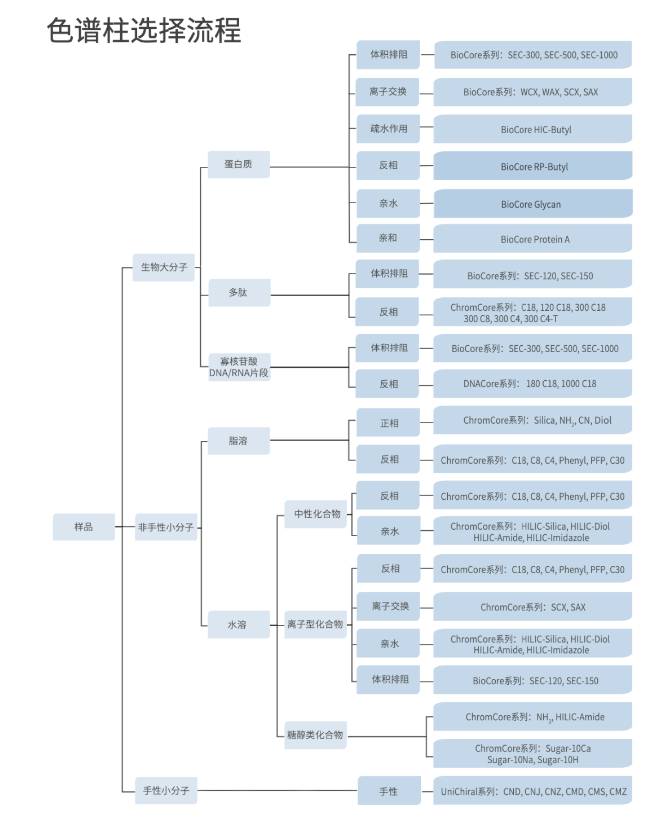
产品快速选择指南
 400-808-3822
400-808-3822
 info@nanochrom.com
info@nanochrom.com